氢键
氢键是如何形成的
如下图所示,电负性极强的原子从氢原子中拉出电子云,这暴露了氢原子的一部分原子核,使原子带部分正电荷。附近分子上的高电负性原子可以与氢原子相互作用,由于氢原子很小,偶极子可以比大多数偶极子-偶极子相互作用更接近彼此。
 Imgur
Imgur
氢键是最强的分子间作用力.这就解释了与同类相比,水的沸点高的原因16类化合物.通常,沸点随着分子质量的增加而增加范德华力.
下列哪种分子能与同类分子形成氢键?
(一)丙酮
(B)氨
(C)氯化氢
(D)甲烷
要形成氢键,一个氢原子直接连接到 , ,或 原子必须与另一个原子发生反应 , ,或 原子。根据上述所给化合物的结构说明,仅(B)氨含有一个直接连接在原子上的氢原子 , ,或 原子。
在上面的例子中,为什么丙酮不与自己形成氢键呢?氢不能从a 基团连着另一个丙酮分子的氧?
在丙酮中,所有的氢都连着碳,而不是氧、氮或其他电负性很强的元素。由于碳和氢具有大致相同的电负性,电子在键中的分布比在氢氧键中的分布更均匀。氢键要求氢被成键直接对一个电负性元素来说,在氢上留下一个大的部分正电荷,可以吸引另一个电负性元素。
水:氢键如何使地球上的生命成为可能
沸点有增加的趋势分子量增加。注意第16组和第17组卤化物的总体趋势,忽略每一行中的第一个点。沸点从一组原子中最轻的原子到最重的原子以近似线性的方式增加。形成氢键的化合物( )不遵循模式。它们的沸点明显更高,尽管它们的分子量最小氢化物在它们各自基团中的。这种异常是氢键的直接结果。如果用16组其他物质的趋势线来推断,水的沸点应该在 而不是
每个水分子都有两个氢原子和两对未共享电子,这使得水分子可以参与四个氢键。的四面体电子排布导致每个分子上的氢键在空间上与该分子上的其他键分离,导致典型的分子中非常松散的分子包装晶体结构冰。因此,固态冰的密度低于液态水的密度。
当一个湖泊在冬天结冰时,首先在湖面上形成冰层,因为冰的密度较小。地表下的液态水在表层经历这一过程时保持着稳定的温度相变使湖中的植物、动物、昆虫和微生物得以过冬。如果冰的密度比水大,并沉到湖底,湖水最终会冻结成固体,保证了池塘生物的短暂生命和春天的可怕景象。
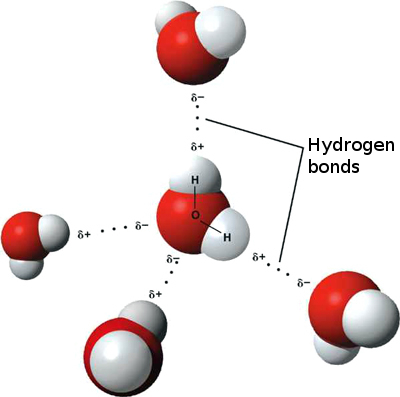 水分子间氢键的三维模型。氢键通常用虚线表示。[3]
水分子间氢键的三维模型。氢键通常用虚线表示。[3]
参考文献
- Baaden, M。使用HyperBalls的动态水氢键网络.从检索https://www.youtube.com/watch?v=pBK22hN7cIM
- Jkwchui。沸点,卤素.从检索https://commons.wikimedia.org/wiki/File:Boiling-points_Chalcogen-Halogen.svg
- 波尔图,。3 d_model_hydrogen_bonds_in_water-es.jpg.从检索https://commons.wikimedia.org/wiki/File:3D_model_hydrogen_bonds_in_water-es.jpg



