分子间力的强度
约旦平静而且克里斯托弗•威廉姆斯做出了贡献
分子间作用力是两个不同化合物或分子之间的吸引力和排斥力。它们包括伦敦色散力,偶极子相互作用,氢键.分子间力影响化合物的许多性质,如蒸气压和沸点。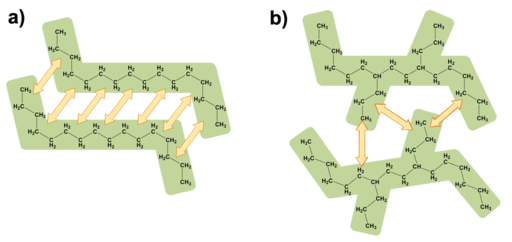 化合物的结构可以影响分子间力的形成和强度。与直链烷烃相比,支链烷烃形成伦敦色散力的机会更少。[1]
化合物的结构可以影响分子间力的形成和强度。与直链烷烃相比,支链烷烃形成伦敦色散力的机会更少。[1]
相比之下,内部分子力是指包含在单个原子或分子内的力,例如碳原子内电子与环绕它运行的原子核之间的吸引力,或者一个电子与形成单个一氧化碳分子的共价键中的两个原子核之间的吸引力。
分子间作用力的强度,从弱到强排列:伦敦色散<偶极-偶极<氢键
有时,一种化合物有不止一种分子间作用力。例如,水具有伦敦色散、偶极子-偶极子和氢键。 氯化钠的单位电池显示出排列有序、排列紧密的离子。公共领域的形象。
氯化钠的单位电池显示出排列有序、排列紧密的离子。公共领域的形象。
注意,氯化钠晶体有一个统一的,可预测的模式,没有明确的边界。相比之下,冰晶有不同的分子,它们之间的联系更紧密。水样本中的氧原子对组成自己分子的两个氢原子的吸引力(分子内力)比对附近其他氢原子的吸引力(分子间力)更强。
参考文献
- Danielchemik。伦敦在烷烃中的力量.从检索https://commons.wikimedia.org/wiki/File:London_Forces_in_alkanes.png
引用:分子间力的强度。Brilliant.org.检索从//www.parkandroid.com/wiki/strength-of-intermolecular-forces/
