相变
相变当物质改变能量状态时发生的物理变化,但化学键没有破碎或形成。
例如,即使它们都是冰,液体水和蒸汽的物理性质也是完全不同的 物质的分子结构也没有区别。
物质的阶段取决于能量的量原子包含。所有原子都在运动。原子的温度越高,运动越快。虽然您的眼睛无法检测到这一点,但仍振动。液体形式允许原子彼此滚动,但不会从容器中反弹。气体具有如此高的能量状态,即分子实际上是在容器中弹出并占据允许它们的空间。能量水平越高,原子移动的速度越来越远。
阶段定义
![荧光灯使用低压将气体变成等离子体。在该灯中,气体是氩气。[1]](https://ds055uzetaobb.cloudfront.net/brioche/uploads/mMz4E8u498-bell_jar_35_with_argon_plasma.JPG?width=1200)
固体通常是结晶的,这意味着它们有一个重复的,有序的三维结构。两种最常见的晶体是金属晶体和离子晶体.金属固体由金属原子组成紧密填充在一起。它们往往具有高熔融和沸点。金属通常良好地进行电,因为它们的外电子自由地从原子移动到原子。离子固体是正极和带负电离子的聚集体。表盐,NaCl是一个常见的例子。离子晶体也具有高熔点和沸点,但它们通常是较差的电力导体,因为化合物在正电荷和带负电的离子之间具有强的静电相互作用。
颗粒在液体它们靠得很近,使这个阶段难以压缩或膨胀,但粒子并不像固体那样固定。它们可以彼此滑动,使液体有可能改变形状,并与另一种液体甚至是处于不同相的物质混合。这个属性很重要,因为它允许液体形成解决方案。这些两种或两种以上物质的均匀混合物是许多化学反应发生的地方。两种液体混合的程度称为它们的混合程度混溶性。油和水是高度非混相它们的分子会相互排斥。
气体可以说是物质中最不复杂的相,因为所有的气体都表现出相似的行为,遵循同样的定律,比如理想气体定律,无论身份如何。气体颗粒非常迅速地移动并且彼此的物理相距远远远,因此颗粒之间存在弱的分子间力。这些特性使气体流体在其形状和体积中,并且相对容易压缩。
 共同阶段总结
共同阶段总结
相平衡
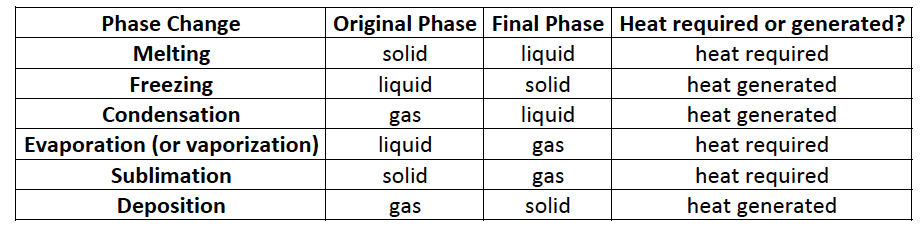 相变总结相变度是可逆的,并且在某些条件下的相位之间存在平衡。例如,液体固体平衡水点为1个atm和
.在这些条件下,一个冰块漂浮在一杯水中,会不断地发生相变(一些冰吸收热量并融化,一些水释放热量并冻结),但固体与液体的相对比例保持不变。
相变总结相变度是可逆的,并且在某些条件下的相位之间存在平衡。例如,液体固体平衡水点为1个atm和
.在这些条件下,一个冰块漂浮在一杯水中,会不断地发生相变(一些冰吸收热量并融化,一些水释放热量并冻结),但固体与液体的相对比例保持不变。
![液态二氧化碳,也被称为干冰,经历升华。它通常被用作制冷剂。[2]](https://ds055uzetaobb.cloudfront.net/brioche/uploads/ApgaGH0mfb-dry_ice_in_cup.jpg?width=1200) 液态二氧化碳,也被称为干冰,经历升华。它通常被用作制冷剂。[2]液体的温度是由其分子的动能决定的。一些分子可能有足够的能量到达液体气体平衡,这时液体蒸发,进入气相。当这些高能粒子进入气相时,降低了液体的平均温度,因此蒸发是一个冷却过程。另一种思考方式是,蒸发需要热量。出汗是实际蒸发的一个例子。与蒸发相反的是冷凝。当气体冷凝时,它移动到一个较低的动能状态,从而产生热量。
液态二氧化碳,也被称为干冰,经历升华。它通常被用作制冷剂。[2]液体的温度是由其分子的动能决定的。一些分子可能有足够的能量到达液体气体平衡,这时液体蒸发,进入气相。当这些高能粒子进入气相时,降低了液体的平均温度,因此蒸发是一个冷却过程。另一种思考方式是,蒸发需要热量。出汗是实际蒸发的一个例子。与蒸发相反的是冷凝。当气体冷凝时,它移动到一个较低的动能状态,从而产生热量。
虽然例子在日常生活中,但是在平衡中也可以存在气体和固体。直接移动到气体的固体升华虽然反向沉着.
相变图
![单个物质的广义相变图。固体绿线显示液体固体平衡的通常形状,而虚线的绿线显示出水的异常行为。[3]](https://ds055uzetaobb.cloudfront.net/brioche/uploads/ncgYqtYA6h-screen-shot-2016-02-15-at-85718-am.png?width=1200) 单个物质的广义相变图。固体绿线显示液体固体平衡的通常形状,而虚线的绿线显示出水的异常行为。[3]
单个物质的广义相变图。固体绿线显示液体固体平衡的通常形状,而虚线的绿线显示出水的异常行为。[3]
相变图显示了在给定温度和压力下物质的内容。的三相点是所有三相可以同时存在的唯一温度和压力。
每种物质都有临界温度这是它作为液体存在的最高温度。另外,每种物质都有一个临界压力,即在临界温度下使物质液化所需的最低压力。临界温度和临界压力的交点叫做临界点。这是气体和液相的密度变得相等的地方。超出该点,这两个阶段难以区分,称为a超临界流体.
改变物质中热能的量通常会引起温度的变化。然而,在相变过程中,即使热能发生变化,温度也保持不变。这个能量是用来改变相变的而不是用来提高温度的。这就是为什么水在沸腾时不会变热。温度保持不变直到相变完成。
相变和潜热
假设我们有一个纯冰的样品,我们决定加热它。我们用电加热器加热冰块,电加热器以恒定速率提供热量。然后,如果我们测量样本的温度,并绘制其随时间的变化,我们得到一个类似下图的图表。

特定的潜热
不要混淆比热
的特定的潜热相变的是完全改变物质的单位质量相位所需的能量是保持温度恒定的。
特定潜热的单位是
水的蒸发潜热约为 融合的潜热是关于
熔化需要多少能量 冰水 ?
聚变的潜热是 .这意味着我们需要 融化一公斤冰的能量。因为我们想要融化 冰,我们需要 焦耳的能量。
参考
[1]来自https://commons.wikimedia.org/wiki/file:bell罐35和Argon_Plasma.JPG在知识共享许可下重用和修改。
[2]图片来自https://commons.wikimedia.org/wiki/File:Dry冰in_cup.jpg根据Creative Commons许可重复使用和修改。
[3]图片来自https://commons.wikimedia.org/wiki/File:Phase-diag.svg,在知识共享许可下重用和修改。

