杂交
杂交(或杂交)是一个数学上结合两个或两个以上的过程原子轨道从同一个原子形成一个完全不同于其组成部分的新轨道,因此被称为a杂化轨道.
原始的原子轨道在能量上是相似的,但不相等(例如,2s轨道可能与2p轨道杂化)。由此产生的杂化轨道彼此之间的能量是相等的,并且是有方向的,以便它们能与其他原子成键。
![杂化轨道,三维视图[1]](https://d18l82el6cdm1i.cloudfront.net/uploads/A90GKuLVAU-hybridation_sp3-anim_100.gif) 杂化轨道,三维视图[1]
杂化轨道,三维视图[1]
由于杂化轨道模型的局限性和其他模型的相对实用性,有人反对将杂化轨道作为一种理解分子键的方式教授给普通化学学生价电子层电子对排斥理论(VSEPR)。[2]
使用
杂化作用有助于预测分子的形状,特别是在有机化学中。
莱纳斯·鲍林观察到,在四氯化碳这样的化合物中,所有的键角都是一样的(
),尽管电子来自两者2 s和2 p轨道。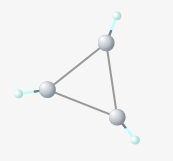 环丙烷的碳-碳键弯曲到大约50度,使分子变得紧张。
环丙烷的碳-碳键弯曲到大约50度,使分子变得紧张。
所有可能的杂化轨道年代和p四面体轨道最适合形成坚固的化学键,”鲍林写道。[1]即使在不对称分子中,四面体碳周围的键角通常在106到113度之间。鲍林接着讨论了不同于四面体值的键角,如环丙烷,并注意到这些键的张力使它们不稳定,因此更容易断裂。

限制
杂化的原子轨道不能准确地预测它们所描述的原子的光谱能量。一些教育工作者认为,这种模式令人困惑,特别是对那些没有学习过英语的学生来说薛定谔方程,不应该在普通化学课程中教授。
参考文献
[1]图片来自https://commons.wikimedia.org/wiki/File:Hybridationsp3-anim100.gif根据知识共享许可协议重用和修改。
(2011)。是时候淘汰杂化原子轨道了吗?j .化学。建造。88(7), 860 - 862。http://dx.doi.org/10.1021/ed100155c
参考文献
- 鲍林,l(1970)。普通化学(页161 - 163)。
