元素周期表
现代元素周期表根据元素的结构将元素组织成网格原子序数.元素在周期表中的水平和垂直位置都提供了有关该元素行为的线索,使元素周期表成为预测某些元素如何相互反应的快速而有用的参考。

阅读元素周期表
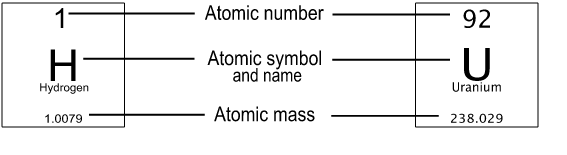
表上的每个框代表一个元素。元素的基本信息包含在每个元素周期表中,包括以下内容:
- 的的名字元素的
- 一个或两个字母原子的象征
- 的原子序数,也就是原子核中质子的数量
- 的相对原子质量以原子质量单位为单位 或者说是AMUs,其中一个AMU等于 一个碳12原子的质量,或约1.66 x 10 公斤 (注意:原子质量和原子量这两个术语经常互换,但它们确实有不同的定义。原子量是根据所有自然发生的原子质量和相对丰度计算出来的同位素一个元素)。
历史
19世纪,欧洲各地的科学家们都在研究同一个难题:弄清观察到的化学元素的行为模式,并发展出一种系统化的方法来组织这些元素。
英国的约翰·纽兰兹、法国的亚历山大·Béguyer·德·Chancourtois、德国的朱利叶斯·洛萨·迈耶和约翰·沃尔夫冈·Döbereiner都是对元素周期表做出贡献的科学家。他们注意到元素之间的趋势和相似性,并开始将它们分成离散的组,其中最著名的是Döbereiner的三和弦和Newlands的八度音。
虽然这些早期分类的特定部分很适合,但没有一个系统容纳了大约60个已知元素。
 门捷列夫的元素周期表于1869年首次发表在德国化学杂志《Zeitschrift fϋr Chemie》上。
门捷列夫的元素周期表于1869年首次发表在德国化学杂志《Zeitschrift fϋr Chemie》上。
这些早期的化学家面临着两个障碍。首先,他们知道还有更多的元素有待发现并被纳入元素周期表。第二,一些公布的有关这些元素的信息被认为是错误的。拼图有缺失的部分,也有破碎的部分,这使得拼图更难拼起来。
俄国化学家门捷列夫经常被称为“元素周期表之父”。1869年,他出版了一个版本,其中63个元素由相对原子质量这表明,当元素按这种方式排列时,某些特征会周期性地重复。
把元素放在桌子上正确的位置有时还需要修正它们的原子质量。有时门捷列夫认为原子质量一定是错误的,因为元素似乎出现的顺序是错误的。例如,他把碲放在碘之前,尽管碲比碘重。碘的性质与氟、氯和溴的性质比与氧、硫和硒的性质更相似,而碲的性质则相反。
门捷列夫的桌子具有令人印象深刻的预测能力。他在桌子上留了一个他认为可以放置未发现元素的空格。他预测了其中五种元素的几种性质,包括原子量、熔点、固体密度和价态。到1875年,法国、德国和瑞典的独立研究人员发现了其中的三种元素(镓、锗和钪),进一步证实了门捷列夫的元素周期表。
现代周期律
现代元素周期表是亨利·莫斯利在1913年发明的。莫斯利是一位年轻的英国物理学家,他对原子的结构进行了研究,并得出了这样的结论原子序数原子核中质子的数量是元素的基本属性,而不是元素的基本属性相对原子质量.这就解释了门捷列夫发现的一些矛盾。例如,碲是52号碘是53号。
莫斯利现代周期定律
元素的性质是其原子序数的周期函数。
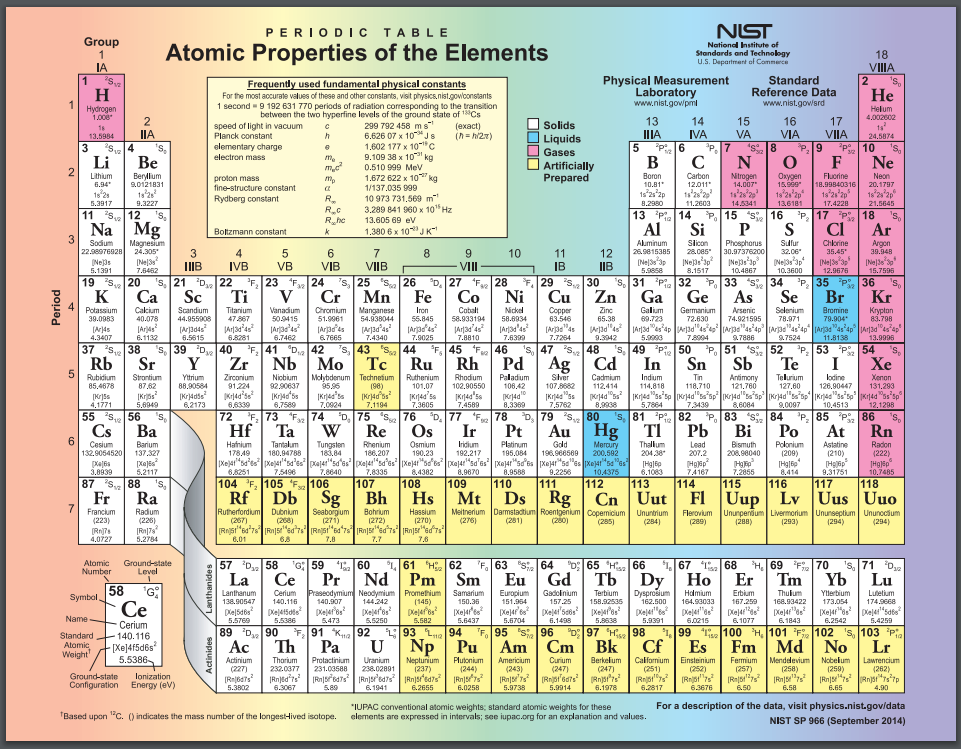 元素周期表可以包含各种额外的信息。这本书讲述了纯元素在室温下的状态,并记录了哪些元素是合成的,而不是在自然界中发现的。来自美国国家标准与技术研究所(NIST)的公共领域图像。
元素周期表可以包含各种额外的信息。这本书讲述了纯元素在室温下的状态,并记录了哪些元素是合成的,而不是在自然界中发现的。来自美国国家标准与技术研究所(NIST)的公共领域图像。
现代元素周期表的优点包括:
- 元素的分类是基于它们原子序数的基本性质。
- 元素的位置是由外层价的电子构型决定的,外层价是将具有相似化学性质的元素自然组合在一起的。
- 惰性气体,已经完全充满价层,被放置在每个周期的末尾。
- 它为金属、非金属、金属类、过渡元素、惰性气体、镧系元素和锕系元素等不同种类的元素提供了明确的界限。
现代元素周期表的不足包括:
- 氢的位置尚未确定。
- 在表的主体部分没有镧系元素和锕系元素的位置。
- 这种排列不能反映过渡族、镧系元素和锕系元素的电子构型。
组
表的垂直列被称为组.基团的最外层或价电子具有相同的电子排布。用罗马数字表示基团数,也就是外层价电子的数目。有两组:A组和b组代表性的元素有价电子在里面 或 子壳层。的非代表性元素B族是过渡金属,已部分填充 亚壳层以及部分填充的镧系元素和锕系元素 子壳层。下面讨论普通化学学生应该熟悉的具有不同性质的组:
期
表的水平行被称为期.一共有7个周期,它们按顺序填充。他们代表着校长量子数 来 .表示句号的时候用的是阿拉伯数字。
周期性是一组元素的相似性质的重复,这些元素被放在一个由一定的原子序数间隔隔开的组中。
换句话说,周期性是指一个群中的元素具有相似的化学性质,因为它们有相同的价层电子配置.所有元素都将获得或失去电子以达到稳定的电子八隅体,惰性气体的价态,导致元素周期表上的一些一般趋势。
从左到右,一次一个电子被加到外层价电子上。外层的电子越多,原子核的吸引力就越强。垂直群的性质也会影响周期趋势。最明显的是,填满的壳层数沿着元素周期表往下增加。外层价电子和原子核之间的电子越多,外层价电子的结合度就越低。这两个因素共同解释了以下问题周期性规律:
原子半径描述原子核周围电子轨道的大小。原子半径减少在一个时间段内从左到右减少在一个组内从下到上。
电离能从原子或离子中除去一个电子所需的能量。电子离原子核越近,就越难移走。电离能增加在一个时间段内从左到右,在一个组内从下到上。
电负性测量原子在形成化学键时吸引电子的强度。电负性增加在一个时间段内从左到右,在一个组内也从下到上。
电子亲和能是一种测量原子接受电子的难易程度的方法。一个正电子亲和能表明当电子被加入时能量被释放。通过观察元素周期表中原子团的价态,可以推广电子亲和能。例如,卤素的电子亲和度很高,因为它们需要一个电子才能形成八隅体,而惰性气体的电子亲和度在0附近,因为它们已经有了一个八隅体。
 周期趋势摘要
周期趋势摘要
元素周期表块
屏蔽效应
镧系收缩
新元素
2015年12月,国际纯与应用化学联盟(IUPAC)宣布,美国、俄罗斯和日本的实验室发现并合成了四种新元素。
有了这些新元素,表的第七周期就完成了。
为元素命名并赋予它们两个字母符号的过程已经完成,这些元素现在被标记为Nihonium (Nh,原子序数113),Moscovium (Mc,原子序数115),tennessee (Ts,原子序数117)和Oganesson (Og,原子序数118)。新元素可以以神话概念、矿物、地点或科学家的名字命名。[1]
其他安排
元素周期表的标准布局并不能捕捉元素之间的所有模式和关系。已经提出了几种替代方案来突出电子构型或量子数,以及其他特性。已经绘制了圆形和三维版本,消除了关于氢的位置以及将镧系元素和锕系元素排除在表的主体之外的一些问题。

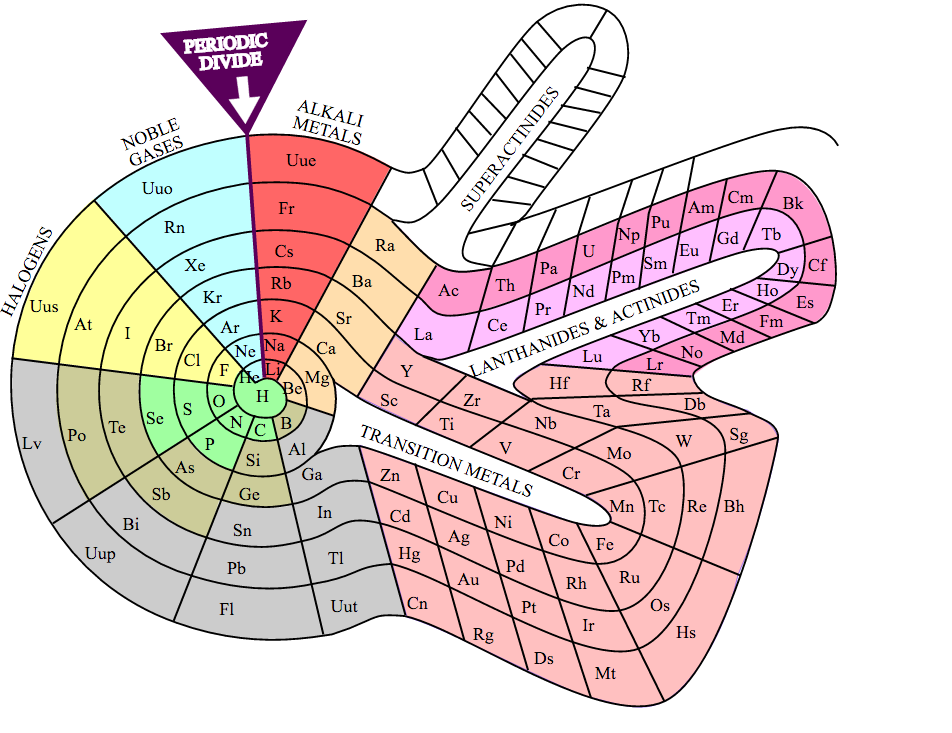 西奥多·本菲的螺旋版式在20世纪60年代首次出版
西奥多·本菲的螺旋版式在20世纪60年代首次出版
交互元素周期表
参考文献
- IUPAC新闻,我。原子序数为113、115、117和118的元素的发现和赋值.从检索http://www.iupac.org/news/news-detail/article/discovery-and-assignment-of-elements-with-atomic-numbers-113-115-117-and-118.html
- 美国洛斯阿拉莫斯国家实验室元素周期表.从检索http://periodic.lanl.gov/index.shtml
- 诺丁汉大学,美国周期性的视频.从检索http://www.periodicvideos.com
