八隅体规则GydF4y2Ba
这个GydF4y2Ba八隅体规则GydF4y2Ba反映了许多元素中最稳定的离子在其价层中有8个电子,以获得可能的最佳稳定性。GydF4y2Ba
氯GydF4y2Ba,例如,通常形成一个负离子,电荷为GydF4y2Ba 虽然GydF4y2Ba钠GydF4y2Ba通常形成带电荷的阳离子GydF4y2Ba .这些模式可以用来预测元素如何结合形成多原子离子和化合物。这些趋势可以用来预测化合物的分子式单位。例如,GydF4y2Ba钠GydF4y2Ba形成盐GydF4y2Ba (一种离子化合物)当它与氯化物结合时,因为它的稳定离子带有电荷GydF4y2Ba ,但镁会形成GydF4y2Ba .GydF4y2Ba
当原子形成共价键时,同样的原理也适用:原子共享电子的方式使两个原子都有一个充满的电子GydF4y2Ba外价GydF4y2Ba,通常包含八个电子。GydF4y2Ba 负离子的电子比中性元素多,而正离子的电子比中性元素少。GydF4y2Ba
负离子的电子比中性元素多,而正离子的电子比中性元素少。GydF4y2Ba
内容GydF4y2Ba
电子解释GydF4y2Ba
最稳定的GydF4y2Ba电子构型GydF4y2Ba对于给定的元素,当最外层发生时(由GydF4y2Ba主量子数GydF4y2Ba)已经满了。GydF4y2Ba
回到引言中列出的例子,氯的外壳中有七个电子,因此氯原子获得一个电子并形成一个封闭的外壳(如阴离子中所示)在能量上更有利GydF4y2Ba )而不是释放七个电子。然后,卤化物离子的电子构型与惰性气体的电子构型相同,紧靠其右侧GydF4y2Ba元素周期表GydF4y2Ba. 同样地,GydF4y2Ba碱金属GydF4y2Ba在一个封闭的壳层外有一个单一的价电子,它们很容易失去这个电子而形成一个阳离子GydF4y2Ba 惰性气体的电荷和电子排布。GydF4y2Ba
唯一的GydF4y2Ba元素GydF4y2Ba在基态有八个价电子的是GydF4y2Ba惰性气体GydF4y2Ba(18)。例如,氖,它有10个电子,它的电子构型如下:GydF4y2Ba 注意有GydF4y2Ba 第二个壳层中的电子,它是最外层的壳层。这同样适用于氩、氪和氙:GydF4y2Ba
注:括号中的电子构型对应于K, L, M, N体系。这三个原子也有相同的事实GydF4y2Ba 最外层的电子。GydF4y2Ba
稳定的八隅体解释了为什么惰性气体很少参与化学反应GydF4y2Ba化学反应GydF4y2Ba.它们在没有获得或失去电子的情况下达到了最大的稳定性。GydF4y2Ba
重复规则GydF4y2Ba

还有另一个规则,叫做双电子规则,它表明某些元素在其壳层中有两个电子时是稳定的。GydF4y2Ba
氢和氦是特殊情况,它们不遵循八重态规则,而是遵循二重态规则GydF4y2Ba 轨道但没有GydF4y2Ba 轨道。它们在双偶态而不是八隅态下是稳定的。GydF4y2Ba
复制规则:GydF4y2Ba
氢和氦填满了它们的最外层,当它们有两个电子时,就达到了稳定的构型。外层价层中有两个电子,而不是八个,不会影响单个原子的稳定性,因为它们只有一个电子GydF4y2Ba1s轨道GydF4y2Ba它最多可以容纳两个电子。这些元素不能达到八隅体状态,因为GydF4y2Bas轨道GydF4y2Ba太小容纳不了吗GydF4y2Ba 有一个高能量势垒将电子加入空壳层。GydF4y2Ba
氢和氦的电子构型如下:GydF4y2Ba
离子形成GydF4y2Ba
自然界中存在的大多数自由单原子离子都遵循八重态规则。单原子离子获得或失去电子,以获得原子序数最接近的惰性气体的电子构型。GydF4y2Ba
钠,或GydF4y2Ba 具有以下电子构型:GydF4y2Ba
如上所述,它的最外层有一个电子。注意,钠离子现在有了电子排布GydF4y2Ba . 这是原子的电子构型GydF4y2Ba 哪一种是原子序数最接近的惰性气体。GydF4y2Ba
氧气,或GydF4y2Ba 具有以下电子构型:GydF4y2Ba
它有GydF4y2Ba 最外层的电子。为了得到稳定的八隅体,一个氧原子可以得到两个电子或失去六个电子。氧的离子形式是GydF4y2Ba 哪个也有电子排布GydF4y2Ba 这和钠离子的电子排布是一样的GydF4y2Ba 这也是原子序数上最接近的惰性气体。GydF4y2Ba
说明钙最可能的离子形式(原子序数20)。GydF4y2Ba
的电子排布GydF4y2Ba 是:GydF4y2Ba
钙有两个价电子。为了得到八个价电子,一个钙原子要么获得六个电子,要么失去两个电子。失去两个电子更为有利,这会产生离子形式的电子GydF4y2Ba ,它的电子排布和GydF4y2Ba
共价键GydF4y2Ba
八隅法则在共价键形成时也适用。电子在原子之间以这样一种方式共享,即每个原子都达到八重态(或双重态)。GydF4y2Ba
A.GydF4y2Ba共价键GydF4y2Ba是一种化学键,其中电子对在两个原子之间共享。这些电子对被称为GydF4y2Ba结合双GydF4y2Ba.它们在分子中的吸引力和排斥力之间创造了一种平衡。GydF4y2Ba

这GydF4y2Ba刘易斯结构GydF4y2Ba说明了共价键。两者GydF4y2Ba碳GydF4y2Ba和GydF4y2Ba氧气GydF4y2Ba碳氧键中的电子在氧原子核和碳原子核的轨道上运行了一段时间。GydF4y2Ba
检查是否GydF4y2Ba (二氧化硫)遵守八位规则。画出GydF4y2Ba点结构GydF4y2Ba确认结果。GydF4y2Ba
所涉及元素的电子构型为:GydF4y2Ba 硫需要两个电子才能达到八电子态。氧也需要两个电子才能达到稳定的构型。GydF4y2Ba因此,硫原子与两个氧原子共用两个电子,形成稳定的共价化合物。这个GydF4y2Ba点结构GydF4y2Ba证实了上述分析。GydF4y2Ba
八重奏规则的例外情况GydF4y2Ba
路易斯结构GydF4y2Ba遵循八隅体规则提供了一个简单的键合模型,对许多化合物都是准确的,但也有例外。GydF4y2Ba
扩展价八位组:GydF4y2Ba
 六氟化硫GydF4y2Ba
六氟化硫GydF4y2Ba
周期3及以上的元素的价电子可以超过8个。八隅体规则是建立在价层有一个八隅体的基础上的GydF4y2Ba 轨道和三GydF4y2Ba 轨道,每个轨道可以容纳两个电子。从GydF4y2Ba ,价壳层也包含五个GydF4y2Ba 轨道可以容纳额外的电子。GydF4y2Ba
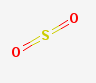 二氧化硫GydF4y2Ba
二氧化硫GydF4y2Ba
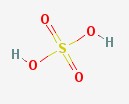 硫酸GydF4y2Ba
硫酸GydF4y2Ba
一个常见的例子是GydF4y2Ba硫黄GydF4y2Ba,即GydF4y2Ba 或GydF4y2Ba 通常情况下,债券比特征债券更具吸引力GydF4y2Ba 这将根据它在第6组中的位置进行预测,其中氧气(氧气主要具有GydF4y2Ba氧化态GydF4y2Ba的GydF4y2Ba ).GydF4y2Ba
例如,当硫与氟结合时,它形成六氟化硫,其中每种卤素都与中心硫原子结合。每个氟原子都有一个八重态,使硫原子总共有12个电子。GydF4y2Ba
其他含硫化合物表现不同。硫原子GydF4y2Ba 债券(GydF4y2Ba 西格玛GydF4y2Ba和GydF4y2Ba 在二氧化硫中,但形式GydF4y2Ba 债券(GydF4y2Ba σ和GydF4y2Ba 在硫酸中。GydF4y2Ba
还有许多其他的例外。锇可以形成8个键!GydF4y2Ba
不完全八位组:GydF4y2Ba
含有非常轻的s-和p-嵌段元素的元素(特别是铍和硼)在没有完全八重体的情况下也可以是稳定的。GydF4y2Ba
八隅体规则和量子力学GydF4y2Ba
在量子力学中,电子有四个量子数,n, l, mGydF4y2Bal, mGydF4y2Bas:GydF4y2Ba
外壳中的所有电子不能共享相同的量子数。GydF4y2Ba
因此,对于GydF4y2Ba ,我们有以下八种可能性GydF4y2Ba :GydF4y2Ba
因此,我们在这里看到一个量子力学证明八隅体规则的例子。GydF4y2Ba

