感应效应,电合效应,共振效应和超共轭
影响有机反应的电子因子包括诱导效应,electromeric效应,共振的影响,超共轭现象.这些电子因素包括有机分子,其中大多数是由以下六种元素的组合构成:碳、氢、氮、氧、磷和硫(统称为CHNOPS).然而,有限的积木数量并不能阻止有机化合物在其物理特性和化学反应性方面具有不同的性质。在有机化学中,各种化合物的细微分化对分子的生物功能至关重要,并产生各种各样的反应。
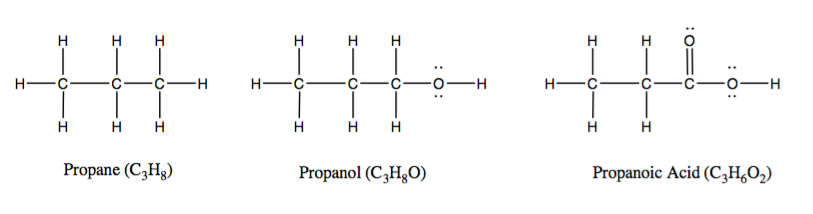
有机化学的这种变化部分源于除了碳和氢之外的其他元素参与分子化学键时电子行为的差异。例如,上图中的三种化合物有相似的结构公式单位和结构,但是由于这些电子因素,它们之间的反应非常不同。不同电负性可能会导致离域效应在这种情况下,一个给定键的电子云扩展到分子内的两个以上原子。
有机分子的极性
部分极性在分子内部,电子会在分子中的原子之间转移,从而导致不同于在非极性版本的化合物中所预期的行为,在非极性版本的化合物中,没有部分是富电子或缺电子的。
饱和烃没有反应性,因为C-C键没有极性,C-H键几乎没有极性。碳和氢几乎完全相同电负性因此,两个原子间成键的电子被两个原子核吸引的程度是一样的,围绕其中一个原子核旋转的时间也大致相同。
电子密度在非极性键的两个原子之间均匀分布,这防止了带电粒子攻击或改变键。相比之下,带电物种(亲电试剂的亲核试剂和)与极性有机分子发生反应,因为电子密度或极性不平衡。
具有较高电负性的元素,包括氧和卤化物集团,可以改变有机分子周围的电子密度,使分子反应性更强。
电子效应使化学反应复杂化,它们可以使分子稳定,使化合物不那么易挥发,使分子更容易以所需的方式反应,或影响酸碱度。理解电子不平衡的相关因素对于理解a的潜在机制至关重要化学反应,预测一个反应的产物和预测有机分子的行为。
电子效果的例子
的诱导效应
共振
内消旋的效果
Electromeric效应
超共轭现象
诱导效应
的诱导效应是一种永久的极化状态。a中的电子密度 两个不同原子之间的键不是均匀的。两个原子的电负性越强,电子密度越高。
归纳效应是一种距离相关的现象:
原子 上面得到一个轻微的负电荷 碳原子带一点正电荷 这意味着键是极化的:
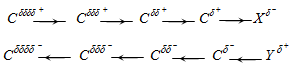
如果电负性的原子 连接到碳原子链上,然后正电荷被传递到其他碳原子上。 ,为正 电荷,对电子施加拉力 ,但两者之间的吸引力要弱于彼此之间的吸引力 在 .这种效应很快就会消失,而且通常不显著 碳原子,或者最多
归纳效应是永久的,但相对较弱,很容易被后面讨论的电子效应所掩盖。
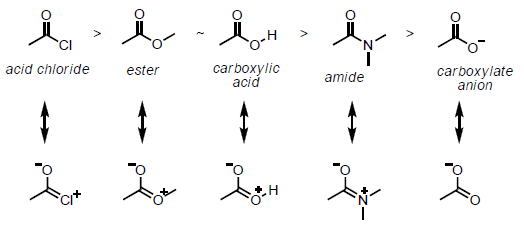
归纳效应分为两类吸电子(-I效应)和electron-releasing我效应(+)。后者也被称为电子基的效果。在上图中, 吸电子和 电子基。
这些相对的感应效应是参照氢来测量的:
我的效果:
-I效应出现在电负性较强的原子或基团周围,那里的电子密度比分子中的其他地方高。吸电子基团包括卤素、硝基 含氰基的 羧基 酯 和芳氧基
+我的效果:
分子中负电性较低的原子通过释放电子(或给电子)基团观察到+I效应。烷基通常被认为是电子释放基(或给电子基)。
共振
有时,有几个是正确的路易斯结构对于一个给定的分子。臭氧 就是一个例子。这种化合物是由三个氧原子组成的链,使每个氧原子的电荷最小化八隅体要求中心氧原子与一端氧形成单键,与另一端氧形成双键。
在画路易斯结构时,双键的位置选择是任意的,任何一种选择都是同样正确的。画路易斯结构的多种正确方法被称为共振形式.
基于共振形式,刚开始学化学的学生可能会想知道臭氧是否有两种不同长度的键,因为单键通常比双键长。然而,臭氧分子是完全对称的,键长相同。没有一种共振形式代表分子的真实结构。相反,形成双键的电子的负电荷是非定域化的或者在三个氧原子上均匀分布。真正的结构是一种复合结构,它的键比单键短,但比双键长。
 通过识别臭氧分子的多重共振结构,发现了臭氧分子的共振杂化。
通过识别臭氧分子的多重共振结构,发现了臭氧分子的共振杂化。
因此,对于 上面所示的两个结构(I和II)构成正则结构或共振结构,它们的杂化(即III结构)代表的结构 更准确。共振用共振结构之间的双头箭头表示,如上所示。
(1)
(2)

共振杂化比其正则形式更稳定,即实际化合物(杂化)处于比其正则形式更低的能态。共振稳定性随共振结构数目的增加而增加。
实验能量和计算能量的差值是使化合物稳定的能量量。这种差异被称为共振能或离域能。
并非所有的共振结构都是等价的。下列规则有助于确定共振结构是否对混合结构有显著贡献。
共振的规则
规则1:最重要的共振贡献者有最多的完整八位元数(或如果适用,扩展八位元)。
规则2最重要的共振贡献者具有最少的形式电荷原子。
规则3:如果形式电荷不能避免,最重要的共振贡献者有负电形式电荷在电负性最强的原子上,正形式电荷在电负性最小的原子上。
规则4共价键的数量最多。
规则5:如果存在键,最重要的共振贡献者在元素周期表中同一行的原子之间有这个键(通常碳与硼、碳、氮、氧或氟成键)。
规则6:芳香共振贡献者比非芳香共振贡献者更重要。
内消旋的效果
与a共轭的基团的永久偏振 键或一组交替键 键是通过 系统的电子,导致电子在不饱和链上的不同分布。这种不饱和化合物中的电子分布与释放电子或吸收电子的基团或原子共轭称为内消旋的效果.
如上所示,在化合物中由于电子的通过而产生极性 债券。这种效应是共振的结果,可以在含有一个双键的化合物中看到,这个双键与另一个双键或一个单键分离的孤对电子。
Electromeric效应
的electromeric效应是由于试剂的攻击,分子内电子从PI键向分子中另一个原子的运动。它是暂时的,是可逆的。
有两种不同类型的电子效应:
(i)正电效应(+E效应)在这种情况下, -多键上的电子被转移到试剂所附着的原子上。例如:

(ii)负电效应(-E效应)在这种情况下, -多重炸弹的电子被转移到攻击试剂没有附着的原子上。例如:

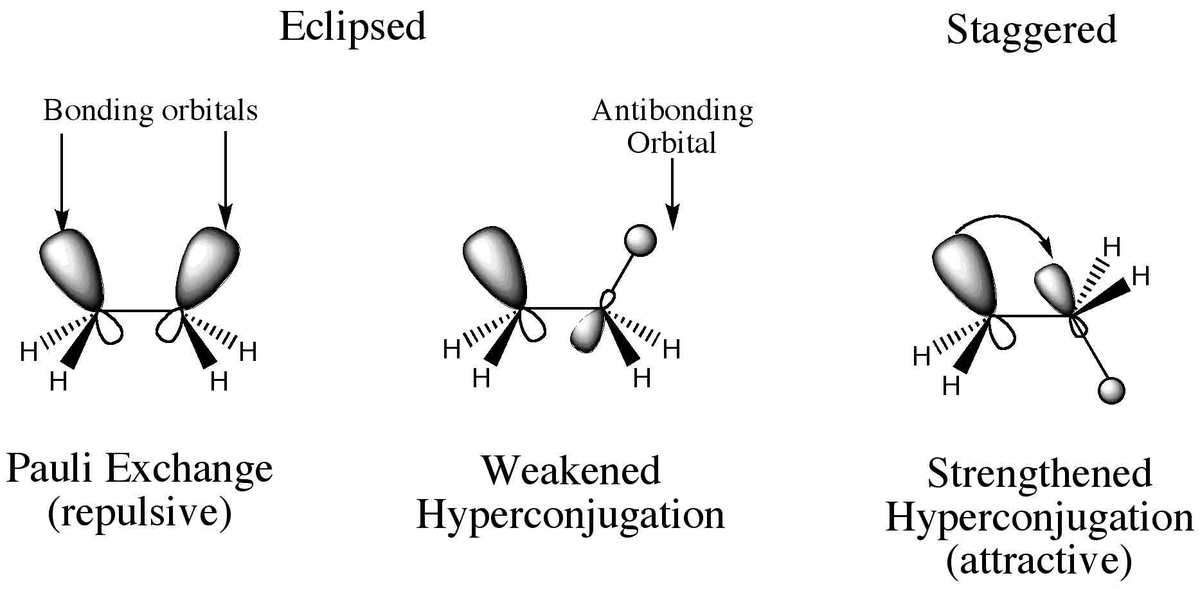
超共轭现象
超共轭现象有助于解释烷基的稳定性激进分子.它涉及到的离域 -电子属于烷基的碳氢键,附在有未共享电子的原子上 轨道。超共轭氢越多,稳定性越好。