路易斯结构
Gilbert N. Lewis引入了一个图解系统来表示价层电子在一个原子。它对我们做化学键很有帮助。他用点来表示价电子。他用线表示两个电子之间的键。这是一个碳的例子,它的价电子路易斯点结构.
代表电子
Gilbert Lewis用点表示价电子。正如上面的例子,你可以看到碳的价电子被表示成点。
但是,当我们要表示两者之间的化学键时不同的原子,我们通常用不同的符号来表示每个参与反应的原子。让我们看一个包含两个不同原子的分子的例子。
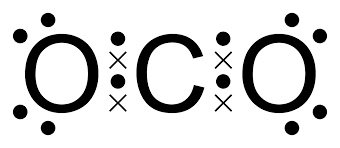
在这种化合物(二氧化碳)中,我们发现氧的电子用点表示,而碳的价电子用叉表示。
注意:如果键是在两个同种原子之间,就没有必要使用不同的符号。
代表债券
我们知道原子趋向于达到八隅体状态(或氢的双极态),并达到稳定。为了获得稳定,原子与其他原子或同一类型的原子结合。为了用图表表示化学键,我们需要知道孤对和结合对.如前所述,(通常)当我们表示化学键时,我们会画一条线,而不是保持键合电子原样。
有时,并不是所有的电子都参与成键;它们远离成键的电子对,而留在原子周围。这些未成键的电子通常是成对的。这种电子被称为孤.
结合对:有一些电子对参与形成键。它们通常用直线表示,以避免与孤对混淆。
这里有一个例子 氨,你可以观察到孤对和成键对:

如前所述结合双以直线表示。但这并不是强制性的;你可以保持键对不变。如上例所示,键合对没有显示为线。但一般来说,我们用直线,这样可以保持整洁。这里有一个例子 (水):
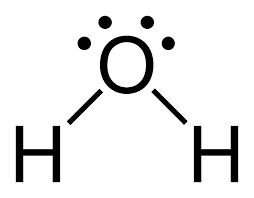
我们可以观察到这两对电子消失了,在它们的位置上放了一条线,表示成键的电子对。线的数目表示成键电子对的数目.
计算孤对和孤键数
对于中性原子,我们看到下面的方程成立:
假设我们要做的是找出分子中键和孤对的数量 .首先,我们来计算惰性气体构型所需的电子总量。这将由 .在哪里 是遵循八隅体规则的常数。对于氢原子, 等于2。对于其他原子, 等于8。 定义为每一种原子的数量。我们用它来说明一下。有1 原子。因此 ,每个原子需要8个电子 ,一个氮原子。有3 原子。因此 ,每个原子需要两个电子。和 ,三个氢原子。
因此,对于 我们可以写:
14个电子是得到稀有气体构型所必需的。每对都包含两个电子,所以有 需要的键和孤对 .
现在我们来看看里面价电子的数量 . 它的外层有5个价电子。这意味着对于我们拥有的“所有”氮原子 总共有价电子。 外层有1个价电子。这意味着我们所有的氢原子 价电子。因此价电子的总量是 价电子。这可以归结为 对(因为我们讨论的是外层的价电子)
这意味着: 当我们检查时,我们发现, 有三个键。剩下的是孤对。它们可以通过减去no来计算。从可用债券中提取。如。 .所以有一对孤对。正如我们所见,这也是正确的。
刘易斯结构的特点
每个键都是a债券这意味着至少两个原子之间共享电子对。
每个键合原子至少贡献一个电子用于共享,正如我们在上面的所有图像中所看到的路易斯点结构.
共用电子的原子这样做是因为需要满足八重位结构(在少数情况下,是双重位结构)。
如果只有一对电子被共用,原子就被a单共价键。
类似的。如果两个电子对共用,原子就被a双共价键。
可以共享的最大电子对是三个.如果是这样的话,原子就被称为a三倍共价键。
