电子构型
原子的电子构型告诉我们电子如何在原子的各个壳层中排列。它给出了其价电子的概念,价电子将决定一个原子如何与其他原子反应。确定电子构型最简单的系统是 系统,由玻尔设计。
据此,原子的壳层被命名为 等,或 等等,所能容纳的最大电子数由公式给出 在哪里 .例如, 外壳可容纳 电子。为了熟悉其价格,请阅读八隅体规则.
波函数的对称性
我们必须为相同粒子的系统构造波函数这样它就能反映出粒子之间无法区分的要求。从数学上讲,这意味着交换占据任意一对状态的粒子不应该改变系统的概率密度。这个简单的陈述具有巨大的后果,它把自然界中的所有粒子分成两类。
两个不相互作用的相同粒子的例子将说明这一点。两个粒子波函数的概率密度必须与已交换的波函数的概率密度相同。
事实上,所有具有半整数自旋的粒子,如电子、质子、中子等,都可以用反对称波函数来描述,并遵循不相容原理。这些粒子被称为费米子,因为它们遵循费米和狄拉克发现的统计分布定律。具有整数自旋的粒子,如光子、α粒子等,用对称波函数描述,不服从不相容原理。这些粒子被称为玻色子,因为它们遵循玻色-爱因斯坦统计。
泡利不相容原理
这个规则指出两个自旋为半整数的粒子不能同时占据相同的量子态。换句话说,在一个轨道上运动的两个电子不能有相同的自旋量子数或简单的自旋。
半整数自旋:自旋是所有基本粒子的固有性质。费米子,构成普通物质的粒子,具有半整数自旋。
例如,在氦原子中,我们有两个电子,它们不存在于同一个自旋中,即氦原子:
注意:自旋量子数有两个值 而且 这意味着电子的自旋可以顺时针表示为 ,或逆时针表示为 .
量子数
主要文章:轨道和量子数.
量子数决定了粒子在特定环境条件下的行为,它们也描述了电子在特定轨道上的行为。根据泡利不相容原理,我们知道两个粒子不能以同一量子态存在,因此存在一组 区分电子量子行为的量子数。他们的名单如下:
1.主量子数:
主量子数指向能量水平电子存在的位置。它用字母表示
的值
自然数。因此,当主量子数的值增加时,能级也会增加,因此值也会增加
指示壳牌(将很快讨论)其中存在电子。例如,
2.角量子数:
角动量量子数是描述形状告诉我们主能层中有哪些亚能层。它用字母表示
,它的值是从哪里来的
来
;也就是说,如果电子的主要量子数是
那么可能的值是
求角量子数的可能值,如果电子在 能量水平。
因为电子在 壳,这意味着它的主量子数的值是 .因此,电子可能的角量子数值将从 来 :
但是这些值代表什么呢?如前所述,它代表亚层(将很快讨论)其中存在电子。
3.磁量子数:
磁量子数告诉我们一个电子所占据的轨道——它决定了一个亚壳层中有多少个轨道以及它们的方向。表示为
它可视化了电子在磁场影响下的行为(比如地球)。
我们知道的运动电荷可以生成磁场在外部磁场的影响下,电子倾向于在原子核周围的特定区域(称为轨道)定向,这就是为什么这个量子数给出了特定亚壳层中的轨道数。磁量子数的值取决于角量子数 .例如,如果一个原子的角量子数是 ,则磁量子数范围为:
所以,有 的值 对于给定的值 ,即会有 轨道。
求一个电子的磁量子数的所有可能值 壳。
如前所述,电子的主要量子数存在于 外壳 .的价值 当 是 .的值 当 将如下:
4.自旋量子数:
在原子物理学中,自旋量子数是一个量子数,它参数化了给定粒子的固有角动量(或自旋角动量,或简单地自旋)。表示为
或者很少像
.人们发现电子不仅围绕原子核旋转,而且还围绕自己的轴旋转,因此自旋量子数有了自己的意义。
显然,电子的自旋只能是顺时针和逆时针两种类型,自旋的值用 当它是顺时针时,和 逆时针方向。有时也用箭头表示:
壳和亚壳
根据量子力学,原子的每个壳层被定义为一个能级。外壳如下:
某一特定壳层中电子的电子排布表示为
在哪里 是原理量子数, 角量子数,和 是电子层的电子数。
 图像来帮助我们记住电子被填满的顺序
图像来帮助我们记住电子被填满的顺序
它还有助于书写任何特定元素的电子构型。例如, - .
构造原理
这个定律说的是电子在进入到较高的能级之前占据了尽可能低的能级。能级增加的顺序由 ,在那里
这个规则是基于原子轨道上节点的总数, ,与能量有关。相等的情况下 值,低的轨道 Value首先被填充。大多数中性原子的基态构型填满了轨道 , 根据元素的光谱特征,通过实验得到了图。
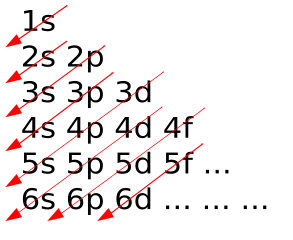 Aufbau原理的图示
Aufbau原理的图示
洪特定律
这为原子中电子的内部排列奠定了基础,它处理的是将电子填入同一亚壳层轨道的顺序。当有不止一个能量相等的轨道可用时(例如: )时,电子首先占据轨道平行旋转或者同样的旋转。只有到那时电子才会配对。
这是因为如果我们把两个自旋相反的电子放在同一个轨道上,排斥性就会增强;然而,如果电子被放置在平行自旋的独立轨道上,斥力就会大大减小。此外,电子占据自旋相同的轨道,从而减少了斥力。
让我们来看看氮和氧的例子:
如果我们遵循氮原子的洪德规则,它的电子构型将是这样的:请注意,电子被放置在具有平行自旋的轨道上,并且在至少一个电子占据每个轨道之前没有配对。
但我们不能将自旋相反的电子放置(如下图所示),也不能在每个轨道至少填满一个电子之前就开始配对电子(如下图所示):
观察未配对电子的总自旋在正确的构型下是最大的,这就是为什么这个规则也被称为洪德最大多重性规则,倍数是电子的自旋,即。 .
氧原子中电子的排列方式遵循洪德定律。电子在 轨道首先被至少一个电子(平行自旋)填满,然后最后一个电子才配对:
而在这个例子中,配对的顺序是错误的,违背了洪德的规则:
再次观察,未配对电子的总自旋在正确的构型中是最大的。
