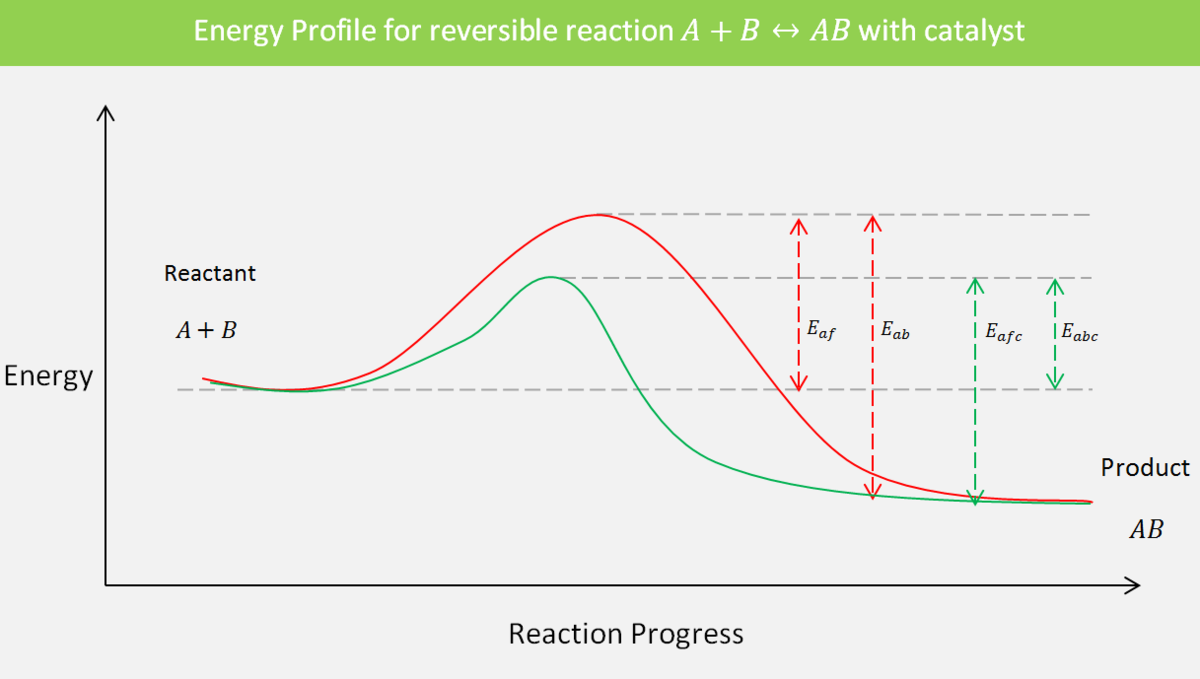
催化剂提高反应速度。催化剂如何做到这一点可以用活化能的概念来解释。我们已经知道活化能代表能势垒。活化能越大,从反应物到生成物的反应越困难。催化剂为反应的发生提供了另一种途径,由一个或几个中间复合物或过渡复合物组成。gydF4y2Ba
我们有必要回忆一下活化能是什么。活化能是过渡态的能量和一个或多个反应物的能量之差。考虑到这一点,逆向反应的活化能将是产物的能量和过渡态之间的差。这是因为在逆向反应中,生成物变成反应物。gydF4y2Ba
让gydF4y2Ba
-
EgydF4y2Ba一个gydF4y2BafgydF4y2Ba为非催化反应中正向反应的活化能;gydF4y2Ba
-
EgydF4y2Ba一个gydF4y2BabgydF4y2Ba是催化反应中反向反应的活化能;gydF4y2Ba
-
EgydF4y2Ba一个gydF4y2BafgydF4y2BacgydF4y2Ba为非催化反应中正向反应的活化能;gydF4y2Ba
-
EgydF4y2Ba一个gydF4y2BabgydF4y2BacgydF4y2Ba是催化反应中反向反应的活化能。gydF4y2Ba
我们来计算一下催化反应和非催化反应的平衡常数。我们有阿伦尼乌斯方程,它把速率常数和活化能联系起来:gydF4y2Ba
kgydF4y2BafgydF4y2Ba=gydF4y2Ba一个gydF4y2BaegydF4y2Ba−gydF4y2BaEgydF4y2Ba一个gydF4y2BafgydF4y2Ba/gydF4y2BaRgydF4y2BaTgydF4y2Ba,gydF4y2Ba
在哪里gydF4y2Ba
一个gydF4y2Ba是指数前因子。gydF4y2Ba
同样,对于逆向反应,gydF4y2Ba
kgydF4y2BabgydF4y2Ba=gydF4y2Ba一个gydF4y2BaegydF4y2Ba−gydF4y2BaEgydF4y2Ba一个gydF4y2BabgydF4y2Ba/gydF4y2BaRgydF4y2BaTgydF4y2Ba.gydF4y2Ba
所以平衡常数由gydF4y2Ba
KgydF4y2Ba=gydF4y2BakgydF4y2BabgydF4y2BakgydF4y2BafgydF4y2Ba=gydF4y2Ba一个gydF4y2BaegydF4y2Ba−gydF4y2BaEgydF4y2Ba一个gydF4y2BabgydF4y2Ba/gydF4y2BaRgydF4y2BaTgydF4y2Ba一个gydF4y2BaegydF4y2Ba−gydF4y2BaEgydF4y2Ba一个gydF4y2BafgydF4y2Ba/gydF4y2BaRgydF4y2BaTgydF4y2Ba=gydF4y2BaegydF4y2Ba−gydF4y2Ba(gydF4y2BaEgydF4y2Ba一个gydF4y2BafgydF4y2Ba−gydF4y2BaEgydF4y2Ba一个gydF4y2BabgydF4y2Ba)gydF4y2Ba/gydF4y2BaRgydF4y2BaTgydF4y2Ba.gydF4y2Ba
同样地,在计算催化反应的平衡常数时,我们有gydF4y2Ba
KgydF4y2BacgydF4y2Ba=gydF4y2BaegydF4y2Ba−gydF4y2Ba(gydF4y2BaEgydF4y2Ba一个gydF4y2BafgydF4y2BacgydF4y2Ba−gydF4y2BaEgydF4y2Ba一个gydF4y2BabgydF4y2BacgydF4y2Ba)gydF4y2Ba/gydF4y2BaRgydF4y2BaTgydF4y2Ba.gydF4y2Ba
自gydF4y2Ba
EgydF4y2Ba一个gydF4y2BafgydF4y2Ba−gydF4y2BaEgydF4y2Ba一个gydF4y2BabgydF4y2Ba=gydF4y2BaEgydF4y2Ba一个gydF4y2BafgydF4y2BacgydF4y2Ba−gydF4y2BaEgydF4y2Ba一个gydF4y2BabgydF4y2BacgydF4y2Ba,gydF4y2Ba
KgydF4y2Ba=gydF4y2BaKgydF4y2BacgydF4y2Ba.gydF4y2Ba